Rumus Umum Senyawa Alkena

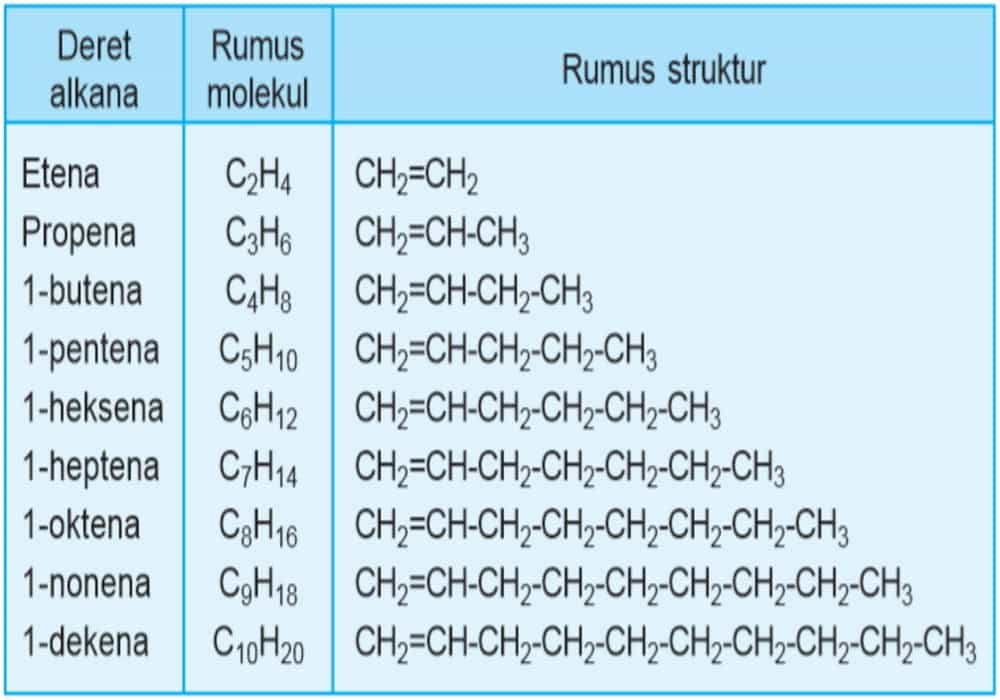
Senyawa alkena adalah hidrokarbon tak jenuh yang memiliki ikatan rangkap dua antara dua atom karbon. Rumus umum senyawa alkena adalah CnH2n, di mana n adalah jumlah atom karbon dalam molekul.
Contoh Senyawa Alkena
- Etena (C2H4)
- Propena (C3H6)
- Butena (C4H8)
Perbedaan Rumus Umum Alkena dengan Senyawa Hidrokarbon Lainnya
Rumus umum alkena berbeda dengan senyawa hidrokarbon lain, seperti alkana dan alkuna. Berikut perbandingannya:
| Jenis Hidrokarbon | Rumus Umum |
|---|---|
| Alkana | CnH2n+2 |
| Alkena | CnH2n |
| Alkuna | CnH2n-2 |
Tata Nama Senyawa Alkena
Tata nama senyawa alkena menurut IUPAC (International Union of Pure and Applied Chemistry) mengikuti aturan-aturan berikut:
Rantai Utama
– Pilih rantai karbon terpanjang yang mengandung ikatan rangkap dua.
– Rantai ini disebut rantai utama.
Penomoran Rantai
– Beri nomor pada rantai utama dimulai dari ujung terdekat ikatan rangkap dua.
Nama Dasar
– Nama dasar senyawa alkena diambil dari jumlah atom karbon dalam rantai utama.
– Akhiran “-ena” ditambahkan pada nama dasar untuk menunjukkan adanya ikatan rangkap dua.
Cabang dan Substituen
– Jika terdapat cabang atau substituen pada rantai utama, beri nama dan nomor cabangnya.
– Nama cabang ditulis di depan nama dasar, diikuti nomor karbon yang mengikat cabang tersebut.
Contoh
– Etena (C2H4): rantai utama terdiri dari 2 atom karbon dengan ikatan rangkap dua.
– Propena (C3H6): rantai utama terdiri dari 3 atom karbon dengan ikatan rangkap dua.
– 2-Metil-2-butena (C5H10): rantai utama terdiri dari 5 atom karbon dengan ikatan rangkap dua pada karbon nomor 2. Terdapat cabang metil pada karbon nomor 2.
Sifat Fisika dan Kimia Senyawa Alkena
Senyawa alkena memiliki sifat fisika dan kimia yang unik karena ikatan rangkap dua karbon-karbonnya. Sifat-sifat ini memengaruhi perilaku dan reaktivitas alkena.
Sifat Fisika
Secara umum, alkena bersifat nonpolar dan tidak larut dalam air. Titik didih dan titik lelehnya lebih rendah daripada alkana dengan jumlah atom karbon yang sama karena gaya van der Waals yang lebih lemah antara molekul alkena.
Sifat Kimia
Ikatan rangkap dua pada alkena sangat reaktif dan dapat bereaksi dengan berbagai reagen. Reaksi yang paling umum adalah reaksi adisi, di mana atom atau gugus fungsi ditambahkan ke ikatan rangkap dua.
- Reaksi Adisi Hidrogenasi: Menambahkan hidrogen ke ikatan rangkap dua untuk membentuk alkana.
- Reaksi Adisi Halogenasi: Menambahkan halogen (seperti klorin atau bromin) ke ikatan rangkap dua untuk membentuk dihalida.
- Reaksi Adisi Hidrasi: Menambahkan air ke ikatan rangkap dua untuk membentuk alkohol.
Selain reaksi adisi, alkena juga dapat mengalami reaksi oksidasi, di mana ikatan rangkap dua terputus dan membentuk gugus fungsi lain, seperti keton atau aldehida. Alkena juga dapat berpolimerisasi, membentuk polimer dengan berat molekul tinggi.
Perbandingan dengan Senyawa Hidrokarbon Lainnya
Dibandingkan dengan alkana, alkena memiliki titik didih dan titik leleh yang lebih rendah karena gaya van der Waals yang lebih lemah. Dibandingkan dengan alkuna, alkena memiliki reaktivitas yang lebih rendah karena ikatan rangkap dua pada alkuna lebih reaktif.
Kegunaan Senyawa Alkena
Alkena memiliki berbagai kegunaan dalam berbagai industri karena sifat reaktivitas dan versatilitasnya. Kegunaan utama alkena meliputi produksi plastik, pelarut, dan bahan kimia lainnya.
Bahan Baku Industri Plastik
Alkena, seperti etilena dan propilena, adalah bahan baku utama untuk produksi plastik, seperti polietilena (PE), polipropilena (PP), dan polivinil klorida (PVC). Plastik ini banyak digunakan dalam berbagai aplikasi, termasuk kemasan, konstruksi, dan otomotif.
Pelarut
Alkena yang lebih kecil, seperti etena dan propana, digunakan sebagai pelarut dalam berbagai aplikasi industri, termasuk pembersihan, pelapisan, dan produksi tinta.
Bahan Baku Industri Kimia
Alkena juga digunakan sebagai bahan baku untuk memproduksi berbagai bahan kimia, seperti alkohol, aldehida, dan keton. Bahan kimia ini digunakan dalam berbagai industri, termasuk farmasi, makanan, dan kosmetik.
Reaksi Penting Senyawa Alkena

Senyawa alkena adalah hidrokarbon tak jenuh yang memiliki ikatan rangkap dua antara atom karbon. Senyawa ini sangat reaktif dan dapat berpartisipasi dalam berbagai reaksi, termasuk reaksi adisi, reaksi oksidasi, dan reaksi polimerisasi.
Reaksi Adisi Elektrofilik
Reaksi adisi elektrofilik adalah reaksi di mana elektrofil (spesies yang kekurangan elektron) ditambahkan ke ikatan rangkap dua alkena. Reaksi ini biasanya dikatalisis oleh asam Lewis, seperti H+ atau AlCl3.
Persamaan reaksi:
“`
RCH=CH2 + HX → RCHX-CH3
“`
di mana R adalah gugus alkil, X adalah halogen, dan HX adalah asam halida.
Mekanisme reaksi:
* Elektrofil menyerang ikatan rangkap dua, membentuk ion karbokation.
* Ion karbokation kemudian bereaksi dengan nukleofil (spesies yang kaya elektron), seperti ion halida, untuk membentuk produk adisi.
Reaksi Oksidasi
Reaksi oksidasi adalah reaksi di mana alkena dioksidasi menjadi berbagai produk, tergantung pada kondisi reaksi. Reaksi ini dapat dikatalisis oleh berbagai reagen, seperti KMnO4, H2O2, atau O2.
Beberapa reaksi oksidasi penting antara lain:
* Oksidasi permanganat: Alkena dioksidasi oleh KMnO4 dalam larutan asam untuk membentuk diol.
* Oksidasi ozon: Alkena dioksidasi oleh ozon (O3) untuk membentuk ozonida, yang kemudian dihidrolisis menjadi aldehida atau keton.
* Oksidasi udara: Alkena dioksidasi oleh oksigen di udara untuk membentuk peroksida, yang dapat terurai menjadi berbagai produk.
Reaksi Polimerisasi
Reaksi polimerisasi adalah reaksi di mana molekul alkena bereaksi satu sama lain untuk membentuk polimer, yang merupakan molekul berukuran besar yang terdiri dari banyak unit pengulangan. Reaksi ini biasanya dikatalisis oleh katalis Ziegler-Natta atau katalis logam transisi.
Persamaan reaksi:
“`
n CH2=CH2 → (CH2-CH2)n
“`
di mana n adalah jumlah unit pengulangan dalam polimer.
Mekanisme reaksi:
* Katalis mengikat ikatan rangkap dua alkena, membentuk kompleks.
* Alkena lain kemudian bereaksi dengan kompleks ini, menambahkan unit pengulangan ke rantai yang sedang tumbuh.
* Reaksi ini berlanjut hingga rantai polimer mencapai panjang yang diinginkan.
Senyawa Alkena dalam Kehidupan Sehari-hari
Alkena, senyawa organik dengan ikatan rangkap dua karbon-karbon, memegang peranan penting dalam kehidupan kita sehari-hari. Sifat kimia dan fisikanya yang unik memberikan berbagai kegunaan, mulai dari bahan bakar hingga plastik dan obat-obatan.
Alkena sebagai Bahan Bakar
Alkena, seperti etena dan propilena, merupakan bahan baku utama dalam produksi bensin dan solar. Ikatan rangkap dua pada alkena mudah dipecah, melepaskan energi yang digunakan untuk menggerakkan kendaraan.
Alkena dalam Industri Plastik
Polietilena, salah satu plastik paling umum, dibuat dari etena. Sifatnya yang kuat, ringan, dan tahan lama membuatnya ideal untuk berbagai aplikasi, seperti tas, kemasan, dan pipa.
Alkena dalam Obat-obatan
Banyak obat-obatan mengandung alkena dalam strukturnya. Misalnya, ibuprofen, obat penghilang rasa sakit, memiliki gugus alkena yang berkontribusi pada aktivitas farmakologisnya.
Dampak Positif Penggunaan Alkena
* Sebagai sumber energi dalam bahan bakar, alkena mendukung transportasi dan aktivitas industri.
* Plastik yang terbuat dari alkena menyediakan kemasan yang aman dan tahan lama untuk makanan, obat-obatan, dan produk lainnya.
* Obat-obatan yang mengandung alkena membantu mengobati berbagai penyakit dan meningkatkan kualitas hidup.
Dampak Negatif Penggunaan Alkena
* Pembakaran bahan bakar alkena melepaskan karbon dioksida, berkontribusi pada perubahan iklim.
* Produksi plastik alkena dapat menghasilkan limbah dan polusi.
* Beberapa obat yang mengandung alkena dapat memiliki efek samping dan memerlukan pemantauan medis.







